编者注:本文根据疫苗专家陶黎纳医生的“COVID-19疫苗整装待发,到底要不要接种?———看这篇就够了”文章改编而来,字数减少了,可以节约阅读时间,但关键内容并没有减少,回答了新冠疫苗是否有副作用、到底要不要接种的疑问。另外,世界很多国家领导人如美国总统拜登、以色列总理内塔尼亚胡等,工商界领袖如比尔盖茨都已经接种了新冠疫苗。中国已经有超过1000万人接种新冠疫苗,说明接种新冠疫苗是安全的。
对于非医学专业和生物专业的人群,由于疫苗知识缺乏、疫苗信息不对称等原因,不少人担心新冠疫苗是否安全、有没有副作用?担心的理由主要是:只用1年时间研发出来的疫苗,这样大规模接种,安全性到底可靠么?
在既往的宣传中,一款疫苗至少要5~10年才能研发成功,现在1年速成的COVID-19疫苗要让公众放心,确实很有难度。但是,再难也要尝试,笔者认为,把不同技术路线的COVID-19疫苗的特点讲清楚,才有可能消除公众的恐慌,帮助他们做出理性的选择。
大家都知道,我国在疫情初期就提出了用5条技术路线研COVID-19疫苗的总体规划,这5条技术路线分别是:
◆ 灭活疫苗
◆ 重组蛋白疫苗
◆ 腺病毒载体疫苗
◆ 流感病毒载体疫苗
◆ 核酸疫苗
实际上,这已经是世界上最全面的疫苗研发路线,没有之一。笔者将尝试用最通俗易懂的方式来解释这些路线背后的原理,相信看完以后,大家就会对1年时间开发出一款疫苗比较有信心特别是不那么担心安全性了。
不过,再谈具体疫苗技术前,有一个非常重要、绝大多数公众和医学专业人员都没有意识到的原理,必须先普及。这个原理实在太重要了,对于深刻理解疫苗的作用机制的安全性,有决定性的作用。
这个原理就是:
疫苗其实是站在人体免疫系统这个巨人的肩膀上,疫苗要做的就是尽可能完美模拟微生物,刺激免疫系统产生针对性的免疫力。
这种微生物与免疫系统之间的攻防战,在人类几百万年的进化史中,已经被锤炼得非常成熟。现代医学对这种微生物与人体免疫系统的互动机制,也已经理解得比较透彻,认为基本不会出现意想不到的副作用,这就是疫苗安全性的基础。
虽然针对各种传染病的疫苗种类很多,但它们的作用机制是高度统一的,所以安全性也是大同小异,整体上都非常安全。
只有少数含有活微生物体的活疫苗,即预防结核病的卡介苗和预防小儿麻痹症的脊灰活疫苗,会在极少数情况下发生严重感染,导致死亡或终生残疾。然而,同样是活疫苗,麻腮风疫苗、乙脑活疫苗、甲肝活疫苗、水痘疫苗等则非常安全。
理解了疫苗安全性的内在机制,我们再来看治疗药。
治疗药绝大多数是结构非常复杂的有机化学分子,有些是从动植物里提取出来的,有些则是发明合成出来的。治疗药各有各的作用机制,进入人体后有怎样的代谢过程和生物效应,很难提前预测,所以其安全性风险要远远大于疫苗。
治疗药里最大的悲剧,就是上世纪50年代末的“反应停”导致海豹儿事件。反应停是一种用于治疗孕妇呕吐的药,效果很好,动物试验里也没发现对胎鼠的健康损害。然而,“反应停"会导致人类胎儿的肢体畸短,就像海豹的短肢那样,这种缺陷的宝宝被称为海豹儿。

后来科学家发现,人类和试验鼠类在反应停的某个代谢环节不一样,导致了这种药对人类胎儿的损伤。再后来,美国建立了最严格的药物研发和准入机制,其他国家也基本以美国为标准。目前,严格的动物试验+3期人体临床试验+默认孕妇不建议用药,已经成为全球公认的药物研发流程。
笔者认为,对于化学药采用这样严格的研发流程是非常有必要的,因为人体非常复杂,我们无法预测这种化学物质在人体内会产生怎样的效应或短期、长期损害。
对于疫苗来说,除了活疫苗需要谨慎,非活疫苗的安全性都非常好,所以临床试验的重点在于确定剂量、接种程序和保护效果,安全性并不是重点。即便是1年速成的COVID-19疫苗,业界对其安全性也有很大的把握。
关键原理介绍完了,希望读者能松一口气,下面具体说说不同的疫苗技术路线。
灭活疫苗、重组蛋白疫苗、腺病毒载体疫苗、流感病毒载体疫苗和核酸疫苗,这5条技术路线先要分个类,便于大家理解疫苗设计的原理。这个分类就是:灭活疫苗单独一类,其他4条路线在一起,称为组分疫苗,具体一点就是S蛋白疫苗。
灭活疫苗主要有效成分为灭活的病毒颗粒,包含所有的病毒结构组分,接近或等于天然病毒颗粒,是最易于研制的疫苗种类。
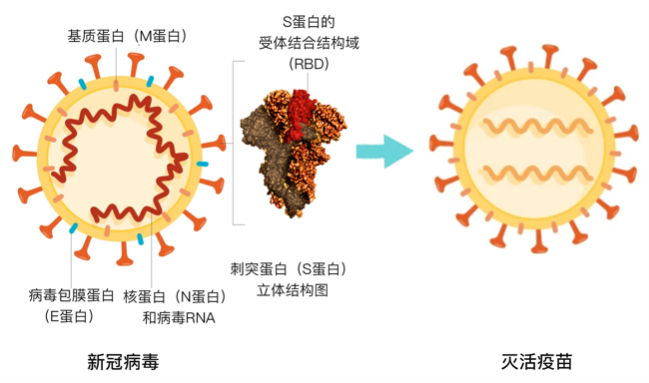
灭活疫苗是一种传统疫苗技术,有120年以上的使用历史(第一个是伤寒灭活疫苗,1896年开始使用),其安全性和有效性得到了充分的验证。
现役疫苗里,无论是儿童常用的脊灰灭活疫苗、甲肝灭活疫苗、乙脑灭活疫苗还是手足口疫苗(只有灭活疫苗),并且是全人群都适用、包括孕妇也不禁忌的狂犬病疫苗(也只有灭活疫苗),都显示出极佳的安全性。
我们知道,活的脊灰病毒会导致永久性瘫痪,活的甲肝病毒会导致黄疸型肝炎、活的乙脑病毒会导致致残性脑炎、活的狂犬病病毒更是世界上最致命的病毒。也就是说,这些病毒活着时,各作各恶,如果把它们弄死了,死样一样一样的,没有实质性区别。
如果要打个比方,比如鸡蛋、鸭蛋、鹌鹑蛋、鸽子蛋,可以孵化出不同的禽鸟,然而如果煮熟了,就没啥区别了,营养成分都差不多,谁也不比谁差,谁也不比谁强,闭着眼睛吃,未必能吃出区别来。
所以,灭活COVID-19疫苗的安全性在一开始就可以预测会很好,实际临床研究也显示确实是目前最安全的技术路线。
下图是笔者整理的5种COVID-19疫苗临床试验中观察到的安全性情况。
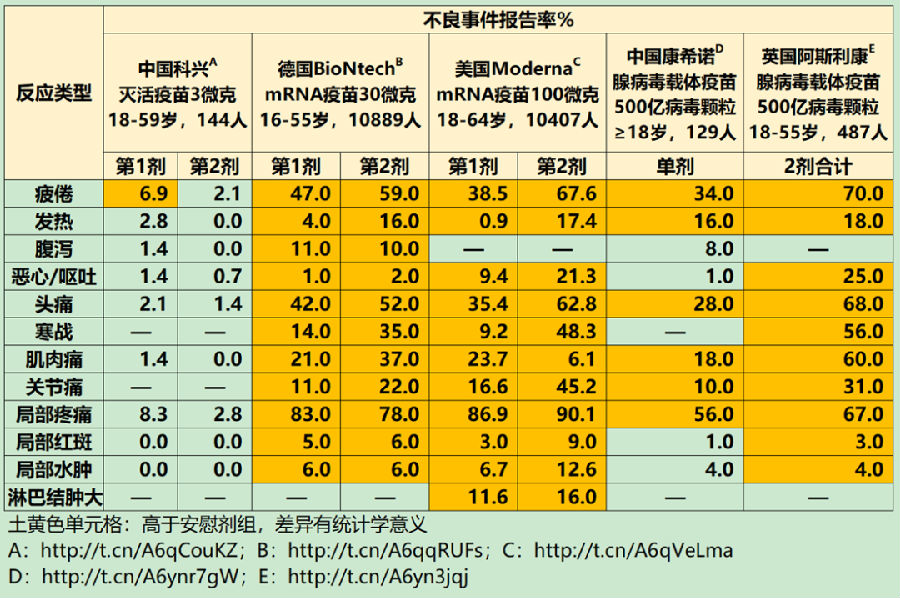
科兴灭活疫苗的不良反应报告率明显低于mRNA疫苗和病毒载体疫苗,更关键的是:科兴的疫苗组不良反应报告率大多与安慰剂组没有差异,只有第1剂的疲倦报告率6.9%高于安慰剂组,所以只能认为该疫苗的真正不良反应只有疲倦,其他都不是。
mRNA疫苗和病毒载体疫苗的不良反应报告率都用土黄色单元格做了标记,那意味着疫苗组的报告率高于安慰剂组,确实都是不良反应。
灭活疫苗有缺点:
一是不能模拟病毒的感染过程,对免疫系统的刺激比较弱,通常只产生以抗体为主的体液免疫;
二是,需要先培养活病原体、再灭活做成疫苗,对生产车间的生物安全等级要求高,产量也受到一定的限制。
灭活疫苗里包含了病毒的全部蛋白,然而这些蛋白全都是免疫力的关键么?
实践证明并非如此。
就COVID-19病毒来说,它至少含有4种结构蛋白(S、E、M、N蛋白)以及更多其他蛋白。
如果S蛋白才是形成免疫关键成分,那么灭活疫苗含有的其他组分蛋白就是多余的,这会导致同等疫苗剂量下,灭活疫苗的S蛋白比例低于S蛋白组分疫苗,可能不利于产生足够强度的免疫反应。同时,其他蛋白就变成了杂质,这让灭活疫苗理论上的不良反应率高于S蛋白组分疫苗。
2003年中国首现的SARS和2012年沙特首现的MERS,让人类对于冠状病毒格外警惕,对这个病毒家族的研究一直在进行。这次的COVID-19病毒,是严重威胁人类的第3种冠状病毒,基于已经开展的大量研究,科学家们几乎认定:病毒表面的S蛋白就是病毒侵入人体细胞的关键蛋白,用这种蛋白做成疫苗,人体产生的S蛋白抗体就可以让S蛋白失去活性,病毒就无法感染人体。
所以,全球来看,选择用S蛋白来研发疫苗的技术路线占据了主流,灭活疫苗其实相对小众。除了中国,还有印度在研发,印度最近已经批准其灭活疫苗紧急使用。
在没有证实S蛋白组分疫苗能提供实质性保护之前,只选择S蛋白疫苗绝对是一种冒险。我国还选择灭活疫苗路线,其实就是怕万一S蛋白疫苗失败,至少灭活疫苗还保留了一丝成功的可能性。
好在选择S蛋白疫苗也是基于科学,并非抓阄乱猜,所以最终两款基于S蛋白的mRNA疫苗都成功了(保护率都达到了95%),这意味着所有S蛋白疫苗都应该可以成功,不成功反而奇怪了,只能怪自己技术不行。
下面就介绍基于S蛋白的其他4几条技术路线。
重组蛋白疫苗的技术相对成熟,目前已经有了很多产品走向市场。
这种疫苗的本质是将编码S蛋白的基因,转基因到某种生产用细胞里,再大量培养这种细胞就能批量生产出S蛋白。收集S蛋白,在进行纯化和添加佐剂等,就成了重组蛋白疫苗。笔者必须强调一下,重组蛋白疫苗是一种转基因疫苗,转基因技术是一种造福人类的技术,妖魔化转基因的做法是反智的。
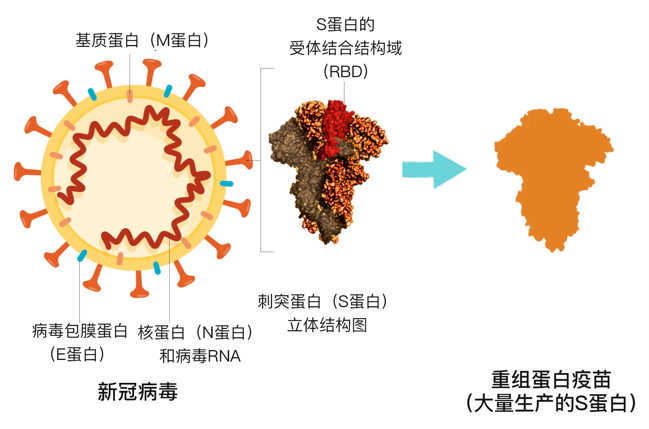
乙肝疫苗是重组蛋白疫苗的鼻祖,已经有30年的应用历史,此外还有戊肝疫苗、宫颈癌疫苗和带状疱疹疫苗。
重组蛋白疫苗目标非常精确,就是病原体的关键蛋白成分,所以它的效果和安全性很可能优于灭活疫苗。其生产过程也不会产生活病原体,对生物安全的要求低,培养细胞来生产病原体蛋白的效率很高,所以产能也高于灭活疫苗。
这两种技术,都是把编码病毒S蛋白的基因,通过转基因技术转入人体细胞,让人体细胞生产出S蛋白,后者刺激人体产生免疫。
区别在于,病毒载体疫苗需要借助腺病毒或流感病毒作为S蛋白基因载体,再将S蛋白基因转入人体细胞;核酸疫苗无需载体,直接把S蛋白基因转入人体细胞。
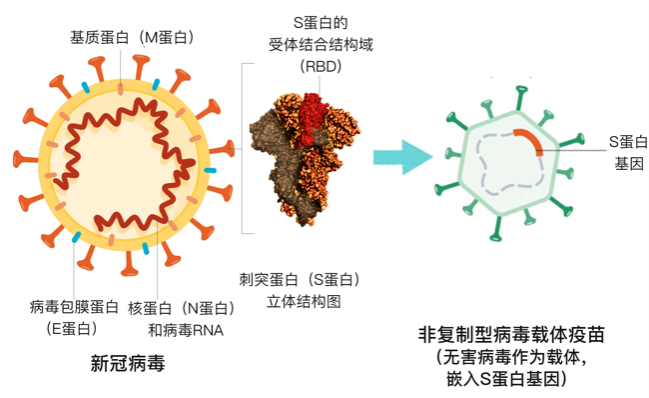
这两种技术路线的疫苗,其实是相当革命性的,因为它们已经不是疫苗,而是“疫苗蓝图/图纸”。
把“疫苗图纸”送入人体,人体就能依照“图纸”生产出疫苗来,确实非常神奇。
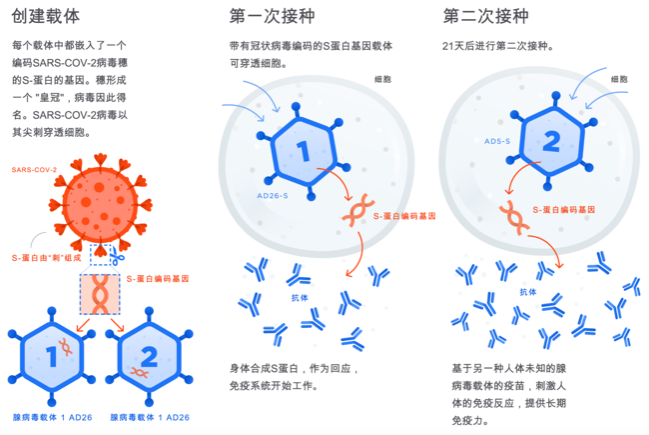
俄罗斯COVID-19疫苗的COVID-19疫苗的双载体技术
核酸疫苗分为mRNA疫苗和DNA疫苗,mRNA会在人体中降解,安全性不用担心:
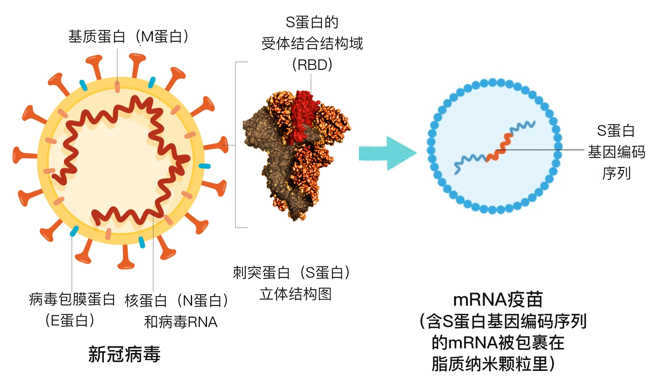
mRNA疫苗作用原理
灭DNA疫苗则有可能整合到人体基因里,其安全性还有待观察,所以进展缓慢。
蓝图/图纸很容易得到,且可以批量复制,所以这两类疫苗在研发效率和生产效率上有可能碾压其他技术疫苗,这是这两种技术最明显的优势,特别是mRNA疫苗。
在应用于COVID-19疫苗前,mRNA疫苗只在不到2000人身上试验过,更没有上市过,所以其安全性和有效性还有待观察。
从已经获批紧急使用的两款mRNA疫苗(德国BioNTech疫苗和Moderna疫苗)来看,有效性已经得到了公认,但安全性方面,其常见的不良反应率明显高于灭活疫苗。
这两款mRNA疫苗还有一个明显的缺点,必须深度冷冻保存。德国BioNTech疫苗需要-70度,Moderna疫苗需要-20度。两者在疫苗标准的冷藏温度2~8度下,只能稳定5天和1个月,其他疫苗通常可以保存2年以上。这两款mRNA疫苗对于非发达国家来说很难企及,对于发达国家来说也要采购低温冷链设备才行。
中国的云南沃森也在研发mRNA疫苗,而且已经实现了2~8度长期保存,这也许是后来者居上吧。
一般认为,mRNA疫苗可以刺激人体的抗体免疫和细胞免疫。抗体免疫可以直接搞定病毒,让人免于感染;细胞免疫可以在病毒入侵细胞后,及时清理感染的细胞并杀死病毒。
在刺激细胞免疫的过程中,人体会有明显的不适。细胞免疫也比较复杂,如果刺激过度则可能影响抗体免疫的效果,甚至导致自身免疫性疾病(比如面瘫和吉兰巴雷综合征)。
如果产生的抗体足够多,病毒一侵入人体被全歼了,没机会感染细胞,细胞免疫就失去了用武之地。现役疫苗的保护效果好不好,绝大多数是用抗体阳性率和抗体浓度去衡量的,很少提到细胞免疫,就是这个道理。
所以,mRNA疫苗需要在细胞免疫方面控制好分寸,如果细胞免疫的保护效果只是锦上添花,但却承包了大多数不良反应,那就应该避免刺激细胞免疫。
好了,5条疫苗技术路线都介绍完了,原理都不复杂,但是骡子是马还是要拉出来溜溜。
从目前批准紧急使用或附条件上市的疫苗来说,都不够完美。灭活疫苗胜在安全性好和冷链适应性强,但保护效果不如mRNA疫苗。mRNA疫苗需要减少不良反应,提高疫苗的温度耐受性。病毒载体疫苗效果不太稳定,不良反应也偏高。
笔者认为,灭活疫苗、病毒载体疫苗和mRNA疫苗都算第一代COVID-19疫苗,解决了从无到有的问题,值得肯定,但进步永无止尽。
第二代疫苗应该在保护效果、安全性和冷链适应性方面取得高水平的平衡,最有希望的就是重组蛋白疫苗,mRNA疫苗经过技术改进也应该可以实现,病毒载体疫苗改进的余地不大,灭活疫苗限于技术原理很难进一步提高保护效果了。
上图为比尔盖茨接种新冠疫苗